1) Reacción de Biuret :
Esta reacción es positiva cuando la molécula contiene dos uniones peptídicas o mas, cercanas entre si (es decir, tripéptidos en adelante). Se realiza tratando la solución a ensayar con CuSO4 en medio alcalino de NaOH.
Las proteínas dan color violeta, las peptonas (PM mayor 5000) color rojo-morado. El color desarrollado se debe a la formación de un complejo de coordinación con el Cu++
2) Reacción xantoproteica:
Se lleva a cabo agregando a la muestra a ensayar (por ej. clara de huevo, o leche) ácido nítrico concentrado en caliente:
La reacción es positiva para prótidos que contienen aminoácidos con anillos aromáticos. En la reacción estos anillos se nitran, por lo que aparece el color amarillo intenso de sus derivados nitrados.
3) Reacción de Hopkins-Cole:
Al realizar la reacción de la muestra de proteinas en medio ácido sulfúrico concentrado , frente al ácido glioxilico (Reactivo de Hopkins-Cole) aparece color violeta en la interfase solución H2SO4, debido a la formación de un colorante similar al índigo.
La reacción es positiva cuando los prótidos poseen aminoácidos con núcleo indólico (Triptofano).
4) Reconocimiento de aminoácidos que poseen azufre:
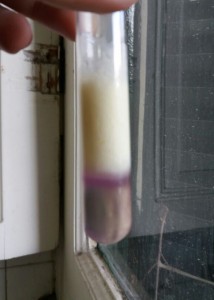
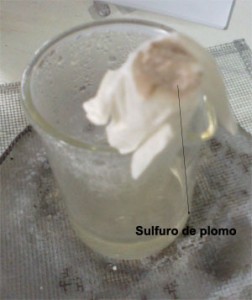
Los aminoácidos sulfurados se descomponen al tratarlos con solución de NaOH en caliente, formando sulfuro de sodio como producto. Éste se pone en evidencia acidificando con un ácido concentrado y colocando en la boca del tubo un papel mojado con acetato de Pb:
Se observa la formación de un sóludo negro-amarronado de sulfuro de plomo:
5) Ensayos de desnaturalización de proteinas:
Si se somete a las proteínas a la acción de ciertos agentes que trastornan su organización, se alteran sus propiedades físicas, químicas y biológicas naturales , y se dice que las proteínas se desnaturalizan. Usualmente, debido a la menor solubilidad en agua de la proteína desnaturalizada se observa la precipitación en la forma de un sólido blanco.
Si se ensaya la albúmina del huevo frente a calor, alcohol etílico, sales neutras (como sulfato de amonio) o a la presencia de un ácido, se observa lo siguiente:
Cuando esto ocurre, las proteinas pierden las estructuras secundaria y terciaria (y cuaternaria si la tuviere).
Autores: María Emilia Pérez, Andrea Amaro, Celina Guiles, Gustavo Pasquale, Federico Ducasse y Diego Ruiz





Muy buena la iniciativa de subir los TP´s en imágenes! Gracias!
cual es la respuesta
Comportamiento de la albúmina en medios como: sales, bases, ácidos
fuertes, ácidos débiles, y alcoholes. buenas ches
El resultado en cada uno de los casos, como se vé en el TP, es la desnaturalización de la albúmina.
Muy interesante todas las prácticas de laboratorios
Excelente conocimiento práctico para entender todo lo referente a los aminoácidos.
En el laboratorio, al realizar el analisis de una muestra, se encuentra que esta es positiva a la reaccion del biuret y negativa a la reaccion xantoproteica . Con estos datos, determina que clase de proteina contiene la muestra
CUAL ES LA RESPUESTA??
No alcanza con eso para identificar la proteína